دکتر ریموند رخشانی *
مقاله و فایل صوتی بیستم:
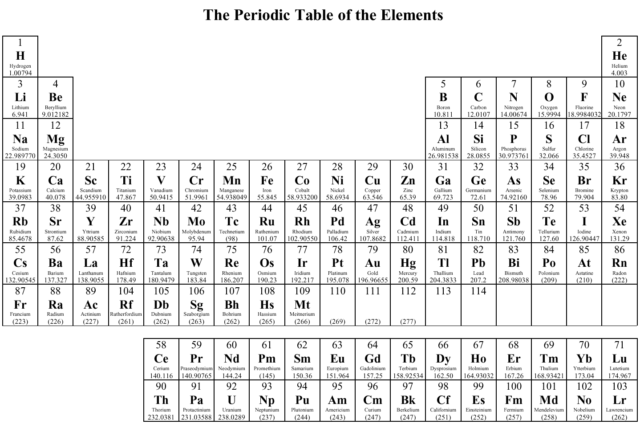
جدولِ تناوبی عناصر[۱]
هَمه ی عناصُرِ شیمیایی در جدولی رده بندی شده اند که گویی زمینِ بازی شیمیدان هاست[۲]. این جدول یکی از شناخته شده ترین جدول هایی است که امروزه در تمامِ کلاس هایِ درسی در همه ی دنیا موردِ استفاده است. اما این جدول هم تاریخِ شکل گیریِ خود را داشته است و به نحوی کامل رده بندی نشد و در آن واحد شکل نگرفت و در واقع محصولِ قرن ها کارِ دستجمعی ای بوده است که هنوز ادامه دارد.[۳]
مدت ها پیش از اثباتِ وجودِ اتم ها بسیاری از پژوهشگران و شیمیدانان متوجه شدند که برخی از عناصر از دیگر عنصرها بنیادین ترند. این “عنصر”ها با هیچ وسیله یِ معمولیِ فیزیکی و یا شیمیایی قابلِ تبدیل به مواد ساده تری نبودند. شناختِ عناصر، پیشینه ی تاریخی ای طولانی دارد.
فرهنگ هایِ کهن حداقل ده عنصر را که در طبیعت موجود بودند می شناختند.
- برخی فلزاتِ قیمتی از قبیلِ طلا، نقره، پلاتینوم و مِس، کمیاب و با ارزش و مشهود بودند اما شیوه ی استفاده از آنها ساده نبود.
- فلزاتِ دیگری از قبیلِ آهن، قلع[۴]، جیوه، آنتیموان[۵] و سرب بسادگی از طریقِ سنگ های معدنی شان با روش های ذوبی[۶] بدست می آمدند.
- برخی غیرفلزها مانندِ کربن (از ذغال سنگ) و گوگرد (از موادِ آتشفشان) از زمان های قدیم شناخته شده بودند.
کیمیاگران قرونِ ۱۲ تا ۱۶ میلادی با استفاده از آتش راهکارِ جداساختن برخی عناصر از قبیلِ آرسِنیک، روی، بیسموت[۷] و فسفر را یاد گرفتند.
بین سالهای ۱۷۳۵ تا ۱۸۰۵ میلادی شیمیدان ها روش هایِ جدیدی را برای خالص سازی[۸] و شناساییِ عناصر بوجود آوردند.
اختراعِ باطری (ابزاری نوین) راهکارِ بسیار مهمِ الکترولیز[۹] را فراهم آورد تا بتوان عناصر را از طریقِ آن تفکیک کرد.
شیمیدان روسی دیمیتری مندلیف[۱۰] (۱۸۳۴-۱۹۰۷) هنگامیکه پژوهش درباره ی جدولِ مشهورِ عناصر خود را شروع کرد ۶۳ عنصرِ شیمیایی را می شناخت. عناصرِ شیمیایی خواص ویژه ی قابلِ اندازه گیری ای[۱۱] دارند که با بکارگیریِ آنها می توان عناصر را به شیوه هایِ متفاوت گروه بندی کرد) نگاه کنید به پی نوشت د. ([۱۲]
- با استفاده از ابزارِ نوین وزنِ نسبیِ عناصر بهنگامِ تجزیه ی ترکیباتِ شیمیایی و محاسبه ی نسبت های وزنی اندازه گیری شدند.
- در حینِ الکترولیز، عناصر خواص یا خصوصیاتِ سیستماتیکی را به نمایش می گذاشتند . برای نمونه برخی عناصر از قبیل اکسیژن، کلر و بروم همیشه به الکترودِ مثبت گرایش داشتند. از آن گذشته گازهایی را که حباب شان در اطراف الکترود شکل می گرفت، میشد جمع آوری کرد.
- فلزات اکثرا بر الکترودِ منفی ) رسوب کرده،( نِهِشتِ رسوبی[۱۳] دارند و دُردِه می بندند. از این اصل برایِ روکش و روپوشش و لعاب دادنِ فلزات در الکترولیز استفاده می شود.
مدتها پیش از مندلیف شیمیدان ها شباهتِ فیزیکیِ ظاهری بعضی عناصر با یکدیگر و همچنین واکنش هایِ یکسانِ شیمیایی برخی عناصر را شناسایی کرده بودند.
- برای نمونه لیتیوم، روبیدیوم[۱۴]، سدیم و پتاسیم همگی فلزاتی نرم و نقرهای رنگ اند و به فلزاتِ قلیایی[۱۵] معروف اند.
- برخی عناصرِ دیگر از قبیلِ بریلیوم، منگنز، کلسیم و باریوم فلزاتِ قلیایی خاکی[۱۶] نامیده می شوند و به نسبتِ ۱ بر ۲ با کلر (مانند CaCl2 ) و با نسبتِ ۱ به ۱ با اکسیژن (مانند CaO سنگ آهک) ترکیب می شوند.
- کلر، بروم و ید غیرفلزاتی بسیار فعال و واکنش دهنده[۱۷] هستند و ترکیباتی شیمیایی با نسبتِ ۱ به ۱ با فلزات قلیایی و ترکیباتی دیگر با نسبتِ ۲ بر ۱ با فلزاتِ قلیایی خاکی می سازند.
بخشی از موفقیتِ مندلیف در بوجودآوردنِ جدولِ عناصرِ خود، در توجه و توانایی او برایِ پیداکردن (برایِ سنتز یا طرح یابی) وجوهِ تشابه خواص یا خصوصیاتِ فیزیکی – شیمیایی عناصر با یکدیگر و عدمِ توجه او به وجوهِ تمایز یا تفاوت[۱۸] آنها ارزیابی شده است.
گروه بندیِ عناصر در جدولِ مندلیف به سادگی موردِ قبولِ دانشمندان قرار گرفت چرا که کارکرد و واکنشِ عناصر را به نحوی آزمون پذیر پیش بینی می کرد و چنین جدول بندی ای با روشِ علمی همخوانی داشت. )نگاه کنید به پی نوشت د(
با بکارگیری ابزارهایی نو کشفِ عناصرِ جدید یکی پس از دیگری موجب گسترش جدول مندلیف شدند.[۱۹]
- اختراع و توسعه ی طیف نمایِ شعله ای[۲۰] سبب کشف عناصر بسیاری بین سالهای ۱۸۷۰ تا ۱۸۹۰ شد. بیش از ۲۰ عنصرِ جدید از جمله عناصرِ کمیابِ زمینی (با وزنِ اتمی ۵۷ تا ۷۱) و همچنین گازهایی که خنثی یا بی اثر (بی کنِش[۲۱]) نامیده می شوند بدین روش کشف شدند.
- جداسازیِ فلورین[۲۲] از چالش هایِ بزرگِ شیمیدان های قرن ۱۹ بود و بالاخره شیمیدانِ فرانسوی هانری موآسان[۲۳] پس از سه سال تلاش و خطر کردن موفق به جداسازی آن شد.
- ماری کوری[۲۴] لهستانی و همسرش پییر با بکارگیری ابزارهای نو نخستین عناصر رادیوآکتیو یعنی پلوتونیوم و رادیوم را در سال ۱۸۹۸ جداسازی کردند. این عناصر به نحوی خودانگیخته از خود اشعه هایی با انرژی بالا گسیل کرده و به عناصری دیگر تبدیل می شوند.[۲۵]
بوجود آمدن الگویِ اتمیِ بوهر موجبِ شناختِ بیشتری از چگونگیِ کارکردِ جدولِ عناصر شد. آن جدول دو شاخصه ی کلیدی عناصر را به نحوی سیستماتیک طبقه بندی کرد: وزنِ اتمی[۲۶] آنها و خواصِ شیمیایی شان را.
- وزن (یا جرم) عناصر در جدولِ مندلیف از چپ به راست و از بالا به پایین افزایش می یابد. راترفورد نشان داده بود که تقریبا همه ی جرمِ هر اتمی باری مثبت دارد و در هسته ی مرکزی آن متمرکز است. افزایشِ وزن رابطه ای مستقیم با اندازه ی هسته ی مرکزی آن اتم و با میزانِ بار مثبتِ آن دارد.
- “شماره یِ اتمی[۲۷]” هر عنصر جایگاهِ آن را در جدولِ مندلیف و تعدادِ پروتون های اش را در هسته ی مرکزی مشخص می کند.
- در مدارهای اتم هایی با باری خنثی تعدادِ کل الکترون ها با تعدادِ کل پروتون های آن اتم در هسته ی مرکزی برابرند. در هر اتمی تعدادِ نابرابری الکترون و پروتون، اتمی باردار (یا یون ها[۲۸]) را می سازد.
عملکردِ شیمیایی هر عنصری بازتابی از درهم کنشِ دو یا بیشتر الکترون، در هر اتم اند.
- خواص یا خصوصیاتِ تناوبیِ عناصر در جدولِ مندلیف نشان می دهند که آن عناصر که عملکردهایی مشابه دارند، چیدمانِ مشابهی هم از الکترون های مدارِ بیرونی دارند. ستون هایِ عمودیِ آن جدول نشان می دهند که آن عناصر چیدمان هایِ مشابهِ الکترونیِ مدارهای بیرونی[۲۹] دارند.
- ستون هایِ افقیِ جدولِ عناصر، در تطابق با مدارهایِ اتمی الکترون ها بدورِ هسته ی مرکزی آنها، چیده شده اند.
- با حرکت از چپ به راست در هر ستونِ افقیِ جدول عناصر، بار مثبتِ هسته یِ مرکزی (تعدادِ پروتون ها) افزایش می یابد. نتیجتاً برای اینکه هر اتمی باری خنثی داشته باشد مدارِ خارجی آن نیز باید افزایشِ الکترونی داشته باشد.
کلیدِ شناخت آنکه اتم ها چگونه در هم ترکیب می شوند در این واقعیت است که “شمارگانِ جادویی[۳۰]” برخی الکترون ها در هر اتمی از شمارگانِ دیگر پایدارتر است. پایدارترین یا باثبات ترین چیدمانِ الکترون ها، دقیقا شمارگانِ ۲، ۱۰، ۱۸، ۳۶ ، ،۵۴ یا ۸۶ الکترون دارند.
می توان به فعل و انفعالاتِ شیمیایی به نحوی نگریست که اتم ها در پیوند یا بهم پیوستگی[۳۱] با دیگر اتم ها، برای ثباتی بیشتر در جستجوی این “شمارگان جادویی” هستند، یعنی چیزی که پیوند یا بهم پیوستگی شیمیایی نامیده می شود. (نگاه کنید به پی نوشت د)
———————————–
The Periodic Table of Elements
Rakhshani, Raymond. Origins of Modernity. Even Development in the Evolution of Science and Technology. South Carolina: CreateSpace, A Division of Amazon Publishing, 2011.
Emsley, J. The Elements, 3rd Edition. New York: Oxford University Press, 1998.
tin
antimony
smelting techniques
bismuth
purify
electrolysis
Dmitri Mandeleev
measurable properties
Levy, P. The Periodic Table. New York: Schocken, 1984.
deposit
Lithium and rubidium
alkali metals
alkaline earth metals
highly reactive
anomalies
Van Spronsen, J.W. The Periodic System of Chemical Elements. New York: Elsevier, 1969.
flame spectroscopy
inert gases
fluorine isolation
Henri Moissan
Marie and Pierre Curie
Pflaum, R. Grand Obsession: Madame Curie and Her World. New York: Doubleday, 1989.
atomic weight
atomic number
Ions
similar arrangements of outer electrons
magic numbers
bonding
————————————
پی نوشت د
جدول تناوبی عناصر شیمیایی
————————————————————–
—————–
* دکتر ریموند رخشانی در باره خودش:
من ریموند رخشانی هستم و حوزه کارشناسی من مهندسی سیستمها است، و تخصص من در بکارگیری اندیشه سیستمی برای انتقال فن آوری و اجرا و پیاده سازی تولید فراوردههای نوین میباشد. در این سلسله از مقالات و فایلهای صوتی کوشش میکنم که علم مدرن را از پایه به دوستان معرفی کنم.

 به کانال تلگرام سایت ملیون ایران بپیوندید
به کانال تلگرام سایت ملیون ایران بپیوندید